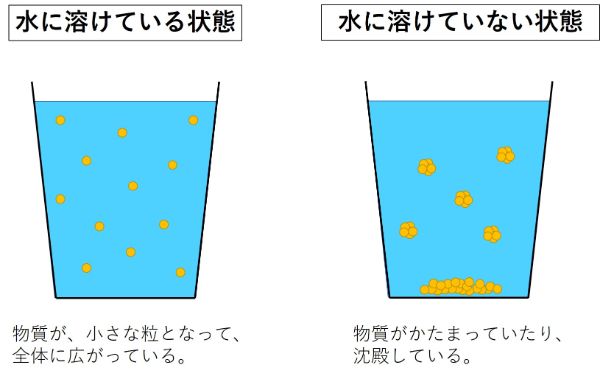
溶質は 、溶媒によって溶解して溶液を作成できる物質 です。
溶質は、気体、液体、固体の形態をとることができます。溶媒、または溶質を溶解する物質は粒子を分散させ、均等に分散させます。これにより、溶液と呼ばれる均一な混合物が生成されます。
溶液中の溶質は、溶質の量を溶液の総体積で割った濃度によって測定されます。
溶媒は、分子間の相互作用の種類に応じて、溶解度の限界に達するまで、ある量の溶質を分散させることができます。
溶質が溶媒に溶解する能力は、 溶解度 として知られています。
溶質の例
最も一般的な種類の溶液は、液体に固体が溶解して形成されるものです。このタイプの溶液の例は、水 (溶媒) 中の塩 (溶質) です。
塩は、溶媒である水に溶解して食塩水を形成する溶質です。一方、ガス中には窒素と酸素がはるかに高い濃度で存在するため、水蒸気は空気中の溶質とみなされます。
他にも解決策の例は無数にあります。たとえば、水中の砂糖、淹れたてのコーヒー、水に溶けた酸素などです。
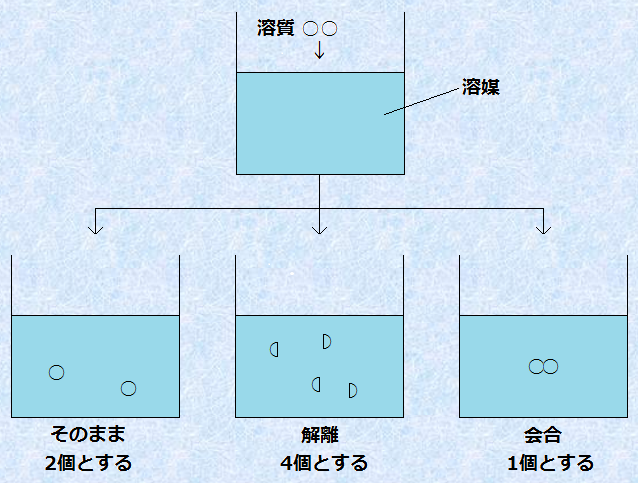
溶液中での溶質の形態とその機能
2 つの物質が混合されて溶液が形成される場合、溶質の割合は少なくなります。溶液は液体、固体、または気体の場合があります。

気体状
酸素やその他のガスは窒素に大量に溶解した溶質であるため、気体溶液の例は空気です。

液体
液体中の液体: 同じ化学的性質を持つが、一定を形成するための濃度が異なる 2 つ以上の物質の混合物。
液体中の固体: 水中の砂糖または水中の塩。

固体
固体中のガス: パラジウムなどの金属に大量の水素が溶解する可能性があります。
液体から固体へ:
- 水銀を金に変え、アマルガムを形成します。
- 水を固体の塩または砂糖にし、湿った固体を形成します。
- パラフィン中のヘキサン。
固体オン固体: 鋼、基本的には鉄原子の結晶マトリックス中の炭素原子の溶液。

飽和溶液と不飽和溶液の違い
飽和溶液とは、所定の温度で最大量の溶質が溶解した溶液です。
簡単に言えば、溶液にそれ以上溶質を溶解できなくなると、溶液は飽和に達します。
簡単に言えば、溶液にそれ以上溶質を溶解できなくなると、溶液は飽和に達します。
参考資料
参考画像一覧








参考動画一覧
【高校化学】溶媒の極性と溶質の溶けやすさ
溶質と溶媒の教え方の違い~先生ととんとん~
【解説授業】中1理科をひとつひとつわかりやすく。 24 溶質+溶媒=水溶液
溶質と溶媒の教え方の違い~先生ととんとん~































